Page 22 - CnO_174
P. 22
9 6A 8 :C IGD H IJ 9> 6CB8D
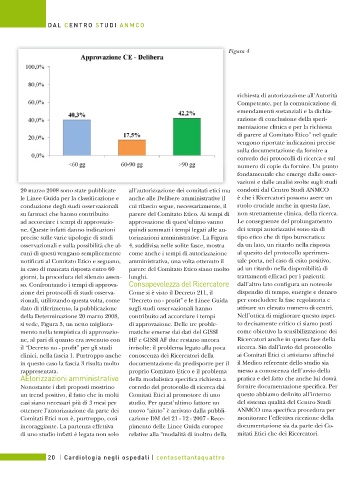
Figura 4
richiesta di autorizzazione all’Autorità
Competente, per la comunicazione di
a
a
emendamenti sostanziali e la dichia-
razione di conclusione della speri-
mentazione clinica e per la richiesta
di parere al Comitato Etico” nel quale
vengono riportate indicazioni precise
sulla documentazione da fornire a
corredo dei protocolli di ricerca e sul
numero di copie da fornire. Un punto
fondamentale che emerge dalle osser-
r
r
vazioni e dalle analisi svolte sugli studi
20 marzo 2008 sono state pubblicate all’autorizzazione dei comitati etici ma condotti dal Centro Studi ANMCO
le Linee Guida per la classificazione e anche alle Delibere amministrative il è che i Ricercatori possono avere un
conduzione degli studi osservazionali cui rilascio segue, necessariamente, il ruolo cruciale anche in questa fase,
su farmaci che hanno contribuito parere del Comitato Etico. Ai tempi di non strettamente clinica, della ricerca.
ad accorciare i tempi di approvazio- approvazione di quest’ultimo vanno Le conseguenze del prolungamento
ne. Queste infatti danno indicazioni quindi sommati i tempi legati alle au- dei tempi autorizzativi sono sia di
precise sulle varie tipologie di studi torizzazioni amministrative. La Figura tipo etico che di tipo burocratico:
osservazionali e sulla possibilità che al- 4, suddivisa nelle solite fasce, mostra da un lato, un ritardo nella risposta
cuni di questi vengano semplicemente come anche i tempi di autorizzazione al quesito del protocollo sperimen-
notificati al Comitato Etico e seguano, amministrativa, una volta ottenuto il tale porta, nel caso di esito positivo,
in caso di mancata risposta entro 60 parere del Comitato Etico siano molto ad un ritardo nella disponibilità di
giorni, la procedura del silenzio assen- lunghi. trattamenti efficaci per i pazienti;
a
a
so. Confrontando i tempi di approva- 8dchVeZkdaZooV YZa G^XZgXVidgZ dall’altro lato configura un notevole
zione dei protocolli di studi osserva- Come si è visto il Decreto 211, il dispendio di tempo, energie e denaro
a
zionali, utilizzando questa volta, come “Decreto no - profit” e le Linee Guida per concludere la fase regolatoria e
dato di riferimento, la pubblicazione sugli studi osservazionali hanno attivare un elevato numero di centri.
t
t
della Determinazione 20 marzo 2008, contribuito ad accorciare i tempi Nell’ottica di migliorare questo aspet-
si vede, Figura 3, un netto migliora- di approvazione. Delle tre proble- to decisamente critico ci siamo posti
a
a
mento nella tempistica di approvazio- matiche emerse dai dati del GISSI come obiettivo la sensibilizzazione dei
ne, al pari di quanto era avvenuto con HF e GISSI AF due restano ancora Ricercatori anche in questa fase della
il “Decreto no - profit” per gli studi irrisolte: il problema legato alla poca ricerca. Sin dall’invio del protocollo
clinici, nella fascia 1. Purtroppo anche conoscenza dei Ricercatori della ai Comitati Etici ci attiviamo affinché
in questo caso la fascia 3 risulta molto documentazione da predisporre per il il Medico referente dello studio sia
rappresentata. proprio Comitato Etico e il problema messo a conoscenza dell’avvio della
6jidg^ooVo^dc^ Vbb^c^higVi^kZ della modulistica specifica richiesta a pratica e del fatto che anche lui dovrà
Nonostante i dati proposti mostrino corredo del protocollo di ricerca dai fornire documentazione specifica. Per
un trend positivo, il fatto che in molti Comitati Etici al promotore di uno questo abbiamo definito all’interno
casi siano necessari più di 3 mesi per studio. Per quest’ultimo fattore un del sistema qualità del Centro Studi
ottenere l’autorizzazione da parte dei nuovo “aiuto” è arrivato dalla pubbli- ANMCO una specifica procedura per
Comitati Etici non è, purtroppo, così cazione DM del 21 - 12 - 2007 - Rece- monitorare l’effettiva ricezione della
incoraggiante. La partenza effettiva pimento delle Linee Guida europee documentazione sia da parte dei Co-
di uno studio infatti è legata non solo relative alla “modalità di inoltro della mitati Etici che dei Ricercatori.
'% q 8VgY^dad\^V cZ\a^ dheZYVa^ q XZcidhZiiVciVfjViigd