Page 21 - CnO_174
P. 21
96A 8 :C I GD H IJ 9> 6CB8D
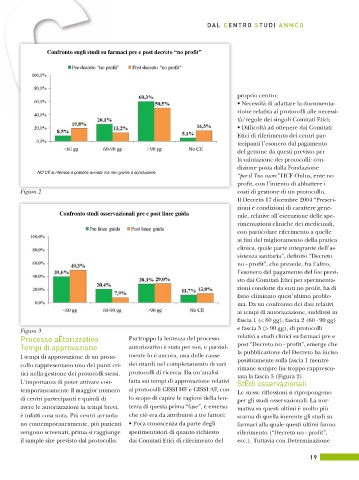
Confronto sugli studi su farmaci pre e post decr
proprio centro;
a
• Necessità di adattare la documenta-
zione relativa ai protocolli alle necessi-
tà/regole dei singoli Comitati Etici;
• Difficoltà ad ottenere dai Comitati
Etici di riferimento dei centri par-
r
r
tecipanti l’esonero dal pagamento
del gettone da questi previsto per
la valutazione dei protocolli: con-
dizione posta dalla Fondazione
NO CE si riferisce a pratiche avviate ma non giunte a conclusione
”
“per il Tuo cuore” HCF Onlus, ente no
profit, con l’intento di abbattere i
Figura 2 costi di gestione di un protocollo.
Il Decreto 17 dicembre 2004 “Prescri-
zioni e condizioni di carattere gene-
Confronto studi osservazionali pre e post linee guida
rale, relative all’esecuzione delle spe-
rimentazioni cliniche dei medicinali,
con particolare riferimento a quelle
ai fini del miglioramento della pratica
clinica, quale parte integrante dell’as-
sistenza sanitaria”, definito “Decreto
no - profit”, che prevede, fra l’altro,
l’esonero del pagamento del fee previ-
sto dai Comitati Etici per sperimenta-
a
a
zioni condotte da enti no profit, ha di
fatto eliminato quest’ultimo proble-
ma. Da un confronto dei dati relativi
ai tempi di autorizzazione, suddivisi in
fascia 1 (< 60 gg), fascia 2 (60 - 90 gg)
e fascia 3 (> 90 gg), di protocolli
Figura 3
relativi a studi clinici su farmaci pre e
EgdXZhhd Vjidg^ooVi^kd Purtroppo la lentezza del processo
IZbe^ Y^ VeegdkVo^dcZ autorizzativo è stata per noi, e parzial- post “Decreto no - profit”, emerge che
la pubblicazione del Decreto ha inciso
I tempi di approvazione di un proto- mente lo è ancora, una delle cause
positivamente sulla fascia 1 mentre
collo rappresentano uno dei punti cri- dei ritardi nel completamento di vari
rimane sempre fin troppo rappresen-
tici nella gestione dei protocolli stessi. protocolli di ricerca. Da un’analisi
tata la fascia 3 (Figura 2).
L’importanza di poter attivare con- fatta sui tempi di approvazione relativi HijY^ dhhZgkVo^dcVa^
temporaneamente il maggior numero ai protocolli GISSI HF e GISSI AF, con
Le stesse riflessioni si ripropongono
di centri partecipanti e quindi di lo scopo di capire le ragioni della len- per gli studi osservazionali. La nor-
r
r
avere le autorizzazioni in tempi brevi, tezza di questa prima “fase”, è emerso mativa su questi ultimi è molto più
a
a
è infatti cosa nota. Più centri arruola- che ciò era da attribuirsi a tre fattori: scarna di quella inerente gli studi su
no contemporaneamente, più pazienti • Poca conoscenza da parte degli farmaci alla quale questi ultimi fanno
vengono screenati, prima si raggiunge sperimentatori di quanto richiesto riferimento (“Decreto no - profit”,
il sample size previsto dal protocollo. dai Comitati Etici di riferimento del ecc.). Tuttavia con Determinazione
&.